北京市西城区2020-2021学年下学期高二年级期末考试化学试卷
本试卷共100分。考试时长90分钟。
可能用到的相对原子质量:H 1 C 12 N 14 O 16
第一部分(选择题
共46分)
每小题只有一个选项符合题意(1~8题,每题2分;9~18题,每题3分)
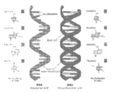
1. 下列物质中,不属于生物大分子的是
|
|
|
|
A. 塑料 | B. 淀粉 | C. 蛋白质 | D. 核酸 |
2. 一种免洗消毒喷剂含酒精75%,它消毒的机理是使细菌和病毒失去生理活性,该变化属于蛋白质的
A. 水解反应 B. 变性 C. 盐析 D. 颜色反应
3. 下列化学用语或模型不正确的是
A. 乙炔的空间填充模型:
B. 羟基的电子式: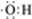
C. 苯的实验式:CH
D. 聚丙烯的结构简式: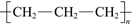
4. 某烷烃的结构简式为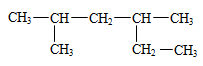 ,其系统命名是
,其系统命名是
A. 2,4-甲基己烷
B. 4-甲基-2-乙基戊烷
C. 2-甲基-4-乙基戊烷
D. 3,5-二甲基己烷
5. 下列说法不正确的是
A. 麦芽糖是具有还原性的二糖
B. 淀粉和纤维素互为同分异构体
C. 氨基酸和蛋白质都具有两性
D. 核酸水解的最终产物是磷酸、戊糖和碱基
6. 下列关于σ键和π键的说法中,不正确的是
A. σ键由原子轨道“头碰头“重叠形成
B. N2分子中的π键为p-p π键,π键不能绕键轴旋转
C. HCl分子中的σ键为s-s σ键
D. p轨道和p轨道之间既能形成π键,又能形成σ键
7. 下列分子或离子中,VSEPR模型和空间结构不一致的是
A. CO2 B. SO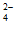 C. BeCl2 D. NH3
C. BeCl2 D. NH3
8. 下列各物质的晶体中,晶体类型相同的是
A. SO2和H2O B. HCl和NaCl C. CO2和SiO2 D. Cu和Ne
9. 下列说法不正确的是
A. PCl3是极性键构成的极性分子
B. H+能与H2O以配位键形成H3O+
C. 分子晶体中,分子间作用力越大,分子越稳定
D. 对固体进行X射线衍射测定是区分晶体和非晶体最可靠的科学方法
10. 氰离子(CN–)和氰[(CN)2]的结构如下图。下列说法不正确的是
氰离子: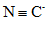
氰: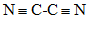
A. CN–中的N原子和C原子上各有1个孤电子对
B. CN–可以作配合物中的配体
C. CN–中N原子和C原子之间形成2个σ键和1个π键
D. (CN)2分子中的4个原子在一条直线上
11. 下列化学方程式书写不正确的是
A. 苯与液溴反应: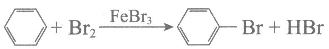
B. 溴乙烷与NaOH的乙醇溶液共热:
CH3CH2Br+NaOH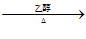 CH2=CH2↑+NaBr+H2O
CH2=CH2↑+NaBr+H2O
C. 向苯酚钠溶液中通入CO2: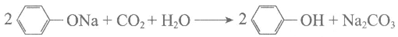
D. 苯酚与甲醛在浓盐酸催化下反应:
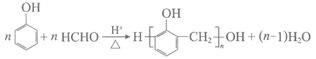
12. 下列事实不能用有机化合物分子中基团间 相互作用解释的是
相互作用解释的是
A. 乙烯能发生加成反应而乙烷不能
B. 苯在50~60℃时发生硝化反应而甲苯在30℃时即可发生
C. 甲苯能使酸性KMnO4溶液褪色而甲烷不能
D. 苯酚能与NaOH溶液反应而乙醇不能
13. 有机化合物X(HOCH2CH=CHCH2OH)是合成维生素B6的中间体。下列关于X的说法不正确的是
A. 分子式为C4H8O2
B. 与HOCH2CH2OH互为同系物
C. 能使溴的四氯化碳溶液褪色
D. 可发生加成、取代、加聚、氧化反应
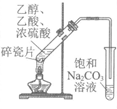
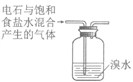
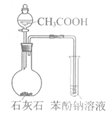
14. 下列实验装置能达到实验目的的是
|
|
|
|
A. 制备并接收乙酸乙酯 | B. 除去乙炔中混有的H2S等杂质 | C. 检验1-溴丁烷的消去产物 | D. 证明苯酚 |
15. 间苯三酚和HCl 甲醇溶液反应生成3,5-二甲氧基苯酚和水。提纯3,5-二甲氧基苯酚时,先分离出甲醇,再加入乙醚进行萃取,分液后得到的有机层用饱和NaHCO3溶液、蒸馏水依次进行洗涤,再经蒸馏、重结晶等操作进行产品的纯化。相关物质的部分物理性质如下表:
甲醇溶液反应生成3,5-二甲氧基苯酚和水。提纯3,5-二甲氧基苯酚时,先分离出甲醇,再加入乙醚进行萃取,分液后得到的有机层用饱和NaHCO3溶液、蒸馏水依次进行洗涤,再经蒸馏、重结晶等操作进行产品的纯化。相关物质的部分物理性质如下表:
物质 | 沸点/℃ | 密度(20℃)/(g·cm-3) | 溶解性 |
甲醇 | 64.7 | 0.7915 | 易溶于水 |
乙醚 | 34.5 | 0.7138 | 微溶于水 |
下列说法不正确 是
是
A. 分离出甲醇的操作是蒸馏
B. 用乙醚萃取后得到的有机层在分液漏斗的下层
C. 用饱和NaHCO3溶液洗涤可以除去HCl
D. 重结晶除去间苯三酚是利用不同物质在同一溶剂中的溶解度不同而将杂质除去
16. 为研究配合物的形成及性质,研究小组进行如下实验。下列说法不正确的是
序号 | 实验步骤 | 实验现象或结论 |
① | 向CuSO4溶液中逐滴加入氨水至过量 | 产生蓝色沉淀,后溶解,得到深蓝色的溶液 |
② | 再加入无水乙醇 | 得到深蓝色晶体 |
③ | 测定深蓝色晶体的结构 | 晶体的化学式为 [Cu(NH3)4]SO4·H2O |
④ | 将深蓝色晶体洗净后溶于水配成溶液,再加入稀NaOH溶液 | 无蓝色沉淀生成 |
A. 在深蓝色的配离子[Cu(NH3)4]2+中,Cu2+提供空轨道,NH3给出孤电子对
B. 加入乙醇有晶体析出是因为离子晶体在极性较弱的乙醇中溶解度小
C. 该实验条件下,Cu2+与NH3的结合能力大于Cu2+与OH–的结合能力
D. 向④中深蓝色溶液中加入BaCl2溶液,不会产生白色沉淀
17. 某柔性屏手机的电池采用有机高聚物做固态电解质,该高聚物的结构片段如下图。下列说法正确的是
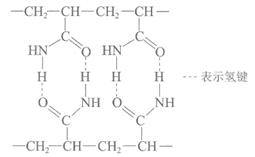
A. 合成高聚物的反应为缩聚反应
B. 氢键对高聚物的性能没有影响
C. 高聚物的单体是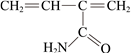
D. 高聚物在NaOH溶液中水解的产物之一是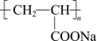
18. 功能陶瓷材料氮化硼(BN)晶体有多种结构。立方相氮化硼是超硬材料,其结构与金刚石相似。六方相氮化硼与石墨相似,具有层状结构,层间是分子间作用力。它们的晶体结构如下图。下列说法不正确的是
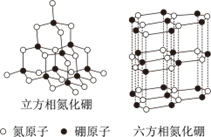
A. 立方相氮化硼属于共价晶体
B. 立方相氮化硼中存在B─N配位键
C. 1 mol六方相氮化硼含4 mol B─N共价键
D. 六方相氮化硼中B原子和N原子的杂化轨道类型均为sp2杂化
第二部分(非选择题
共54分)
19. (10分)甲醇(CH3OH)空气氧化法是生产工业甲醛(HCHO) 常用方法。发生的反应为
常用方法。发生的反应为

(1)C、H、O三种元素的电负性由大到小的顺序为___________。
(2)H2O的中心原子上的孤电子对数为___________。
(3)HCHO分子内σ键与π键个数之比为___________,HCHO的空间结构为___________。
(4)CH3OH和HCHO分子中碳原子的杂化轨道类型分别为___________和___________。
(5)甲醇氧化生成HCHO时,会产生CO、CO2、CH3OCH3等副产物。相同条件下,CO2的沸点比O2的高,主要原因为___________。
(6)工业上利用甲醛易溶于水的性质吸收产品,解释甲醛易溶于水的原因:___________。
20. (8分)金属K和C60能够发生反应产生一系列金属球碳盐KxC60,部分金属球碳盐具有超导性,是球碳族化合物的研究热点之一。
(1)K中含有的化学键是___________键。
(2)C60晶体中分子密堆积,其晶胞结构如下图所示。C60晶体属于___________晶体,每个C60分子周围等距离且紧邻的C60有___________个。
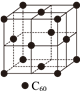
(3)某种KxC60的晶胞结构如下图所示。
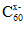 位于立方体晶胞的顶点和面心,K+位于晶胞的体心和棱心,另外晶胞内还有8个K+。
位于立方体晶胞的顶点和面心,K+位于晶胞的体心和棱心,另外晶胞内还有8个K+。
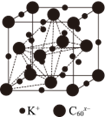
① KxC60中x=___________。
②
该晶胞立方体的边长为a cm,NA为阿伏加德罗常数的值,KxC60的摩尔质量为M g/mol,则晶体的密度为___________g/cm3。
③ KxC60的熔点高于C60,原因是___________。
21. (14分)以玉米淀粉为原料可以制备乙醇、乙二醇等多种物质,转化路线如下(部分反应条件已略去)。F的产量可以用来衡量一个国家石油化工的发展水平。
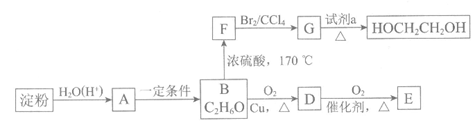
(1)A是不能再水解的糖,A的分子式是___________。
(2)B→F的化学方程式是___________,反应类型是___________。
(3)F→G的化学方程式是___________。
(4)试剂a是___________。
(5)B与E可生成有香味的物质,化学方程式是___________。
(6)可用新制的Cu(OH)2检验D中的官能团,实验现象是___________,化学方程式是___________。
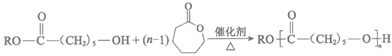
(7)在一定条件下,HOCH2CH2OH与对苯二甲酸( )可发生聚合反应生产涤纶,化学方程式是___________。
)可发生聚合反应生产涤纶,化学方程式是___________。
(8)F能与1,3-丁二烯以物质的量之比1︰1发生加成反应,生成六元环状化合物K,K的结构简式是___________。
22. (12分)药物“肉桂硫胺“的部分合成路线如图所示(部分反应条件已略去):
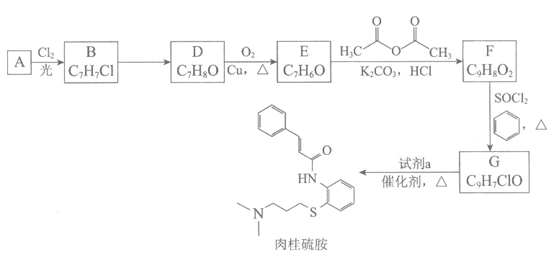
已知: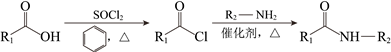
(1)A属于芳香烃,有机物D中所含的官能团的名称是___________。
(2)B→D的化学方程式是___________。
(3)下列关于A的说法正确的是___________。
a. 能使酸性高锰酸钾溶液褪色
b. 分子中所有原子位于同一平面
c. 一氯代物有4种
(4)D→E的化学方程式是___________。
(5)试剂a是___________。
(6)有机物F为反式结构,其结构简式是___________。写出同时符合下列要求的F的所有同分异构体的结构简式___________(不考虑立体异构)。
①
苯环上有2个取代基,核磁共振氢谱显示苯环上有2种不同化学环境的氢原子
②
能与饱和溴水反应产生白色沉淀
③
能发生银镜反应
23. (10分)有机物E可用于合成可降解材料。下图是E的合成路线(部分反应条件已略去)。
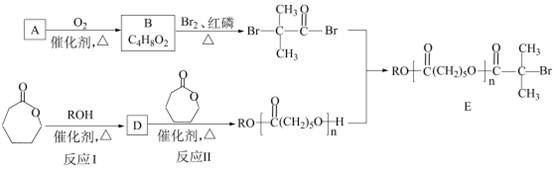
已知:R1COOR2+R3OH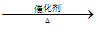 R1COOR3+R2OH
R1COOR3+R2OH
(1)A→B的反应类型是___________。
(2)B能与NaHCO3反应,B的结构简式是___________。B有多种同分异构体,写出一种能发生水解反应的同分异构体的结构简式:___________。
(3)完全燃烧7.2 g有机物A,生成8.96 L CO2(标准状况)和7.2 g水。A物质的蒸气密度是相同条件下氢气的36倍,A的分子式是___________。
(4)反应Ⅰ中,反应物以物质的量之比1︰1发生反应生成D,D的结构简式是___________。
(5)反应Ⅱ的化学方程式是___________。
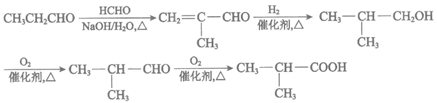
(6)已知:
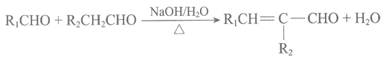
写出由丙醛制备有机物B的合成路线(其他试剂任选)。合成路线示例如下:
CH3CH2OH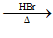 CH3CH2Br
CH3CH2Br
参考答案
1~8题,每题2分;9~18题,每题3分,共46分。
题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
答案 | A | B | D | A | B | C | D | A | C |
题号 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
答案 | C | C | A | B | A | B | D | D | C |
19~23小题,共54分;其他合理答案参照本标准给分。
19. (10分,(5)(6)每空2分,其余每空1分)
(1)O>C>H (2)2 (3)3∶1 平面三角形
(4)sp3 sp2
(5)CO2和O2都属于分子晶体,CO2相对分子质量大,范德华力强
(6)甲醛分子与水分子能形成分子间氢键
20. (8分,(3)①③每空2分,其余每空1分)
(1)金属
(2)分子 12
(3)①3 ②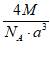
③KxC60是离子晶体,C60是分子晶体,微粒间的作用力离子键强于分子间作用力
21. (14分,(2)~(6)中方程式每空2分,其余每空1分)
(1)C6H12O6
(2)C2H5OH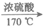 CH2=CH2↑+H2O 消去反应
CH2=CH2↑+H2O 消去反应
(3)CH2=CH2+Br2→CH2BrCH2Br (4)NaOH水溶液
(5)CH3COOH+CH3CH2OH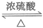 CH3COOC2H5+H2O
CH3COOC2H5+H2O
(6)产生砖红色沉淀CH3CHO+2Cu(OH)2+NaOH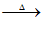 CH3COONa+Cu2O↓+3H2O
CH3COONa+Cu2O↓+3H2O
(7)
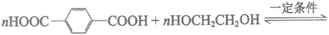
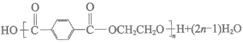
(8)

22. (12分,(1)(5)每空1分,其余每空2分)
(1)羟基
(2)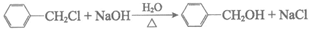
(3)ac
(4)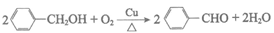
(5)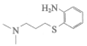
(6)
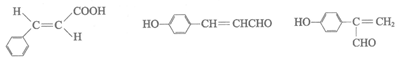
23. (10分,(4)(5)(6)每空2分,其余每空1分)
(1)氧化反应
(2)
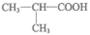
HCOOCH2CH2CH3、HCOOCH(CH3)2、CH3COOC2H5、CH3CH2COOCH3任写一种
(3)C4H8O (4)
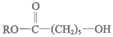
(5)
(6)





 酸性比碳酸的弱
酸性比碳酸的弱