本试卷共24道小题,满分45分。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Ca 40
第一部分 选择题(共12分)
(每小题只有一个选项符合题意。每小题1分)
1. 空气成分中,体积分数约为21%的是
A. H2 B. N2 C. O2 D. CO2
2. 下列不属于化石能源的是
A. 煤 B. 太阳能 C. 石油 D. 天然气
3. 下列符号能表示2个氧分子的是
A. O2 B. 2O C. 2O2 D. 2O2-
4. 下列金属活动性最强的是
A. Mg B. Zn C. Fe D. Cu
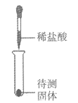
5. 下图所示实验操作中,正确的是
|
|
|
|
A. 取块状固体 | B. 检查装置气密性 | C. 加热液体 | D. 熄灭酒精灯 |
6. “高钙牛奶”中的”钙”指的是
A. 元素 B. 单质 C. 分子 D. 电子
7. 下列说法不正确的是
A. 电器着火用水扑灭
B. 油锅着火用锅盖盖灭
C. 燃气泄漏时应先关闭阀门,再打开门窗通风
D. 室内不宜采用喷洒酒精的方式消毒,易引起爆炸
8. 一些物质的pH范围如下,其中呈碱性的是
A. 柠檬汁(2~3) B. 牙膏(8~9)
C. 西瓜汁(5~6) D. 橘子汁(3~4)
9. 实验室蒸发食盐水,不需要用到的仪器是
A. 蒸发皿 B. 玻璃棒 C. 酒精灯 D. 漏斗
10. 下列实验对应的现象或化学方程式不正确的是
A. 将红热的木炭伸入盛满氧气的集气瓶中:木炭剧烈燃烧,发白光,放热
B. 向滴有酚酞的氢氧化钠溶液中逐滴加入足量盐酸:溶液由红色变成无色
C. 将盐酸滴入盛有镁条的试管中:Mg+2HCl=MgCl2+H2↑
D. 将盐酸滴入盛有氧化铁粉末的试管中:Fe2O3+4HCl=2FeCl2+2H2O
11. 下列实验设计不能达到实验目的的是
选项 | A | B | C | D |
实验设计 |
|
|
|
|
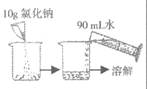
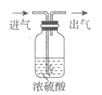
实验目的 | 稀释浓硫酸 | 检验碳酸盐 | 配制100g 10% 的氯化钠溶液 | 除去二氧化碳 中的水蒸气 |
12. 工业上可以将一氧化碳转化为甲烷,反应的微观示意图如下,下列说法不正确的是
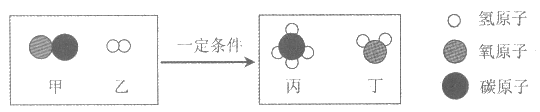
A. 丁的相对分子质量为18 B. 丙中碳、氢原子个数比为1:4
C. 28g甲完全反应至少需要2g乙 D. 反应前后原子种类不变
第二部分 非选择题(共33分)
【生活现象解释】
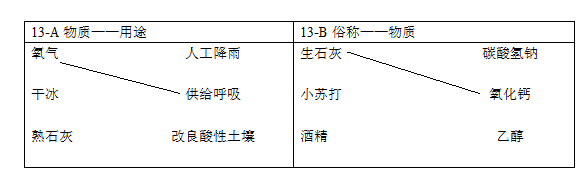
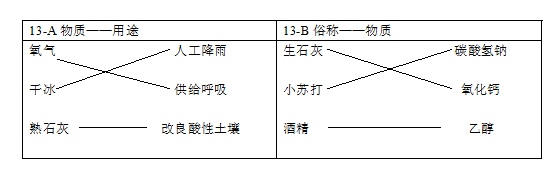
13. (1分)补齐连线。从13-A或13-B中任选一个作答,若均作答,按13-A计分。
 14. (2分)2019年,中国运载能力最大的火箭——长征五号成功首飞,其所用的燃料为液氢。
14. (2分)2019年,中国运载能力最大的火箭——长征五号成功首飞,其所用的燃料为液氢。

(1)液氢属于_______(填序号)。
A. 混合物 B. 纯净物 C. 单质 D. 化合物
(2)火箭中某些核心部件使用特殊钢材,工业上用赤铁矿(主要成分为Fe2O3)和一氧化碳炼铁的化学方程式为_______。
15. (2分)我国口罩日产量从2月初到2月底实现了由不足千万到亿的突破。医用外科口罩,以聚丙烯[(C3H6)n]为主要原料,对细菌、病毒有很强的阻隔作用。
(1)聚丙烯[(C3H6)n]中碳、氢元素的质量比为_________。
(2)关于医用外科口罩的使用,说法正确的是________(填序号)。
A. 可正反面交替使用
B. 使用后,放入指定垃圾桶
【科普阅读理解】
16. (5分)阅读下面科普短文。
藜麦营养成分丰富且比例均衡,被列为”全球十大健康营养食品之一”。
藜麦的蛋白质含量与牛肉相当,且品质不亚于肉源蛋白与奶源蛋白。同时它还含有种类丰富的矿物元素(见图1),以及多种人体所需要的维生素。
藜麦不含胆固醇,富含膳食纤维,能加速肠道蠕动。其脂肪含量与热量都较低,食用后有饱腹感,有利于减肥人群控制体重。
我国很多地区开展了藜麦种植。农业研究小组研究了化肥与藜麦产量的关系。实验数据如表1、图2所示。
表1 化肥用量说明
化肥种类 | 磷肥 | 钾肥 | ||||
符号 | P0 | P1 | K0 | K1 | K2 | K3 |
用量/(千克/公顷) | 0 | 40 | 0 | 40 | 80 | 120 |
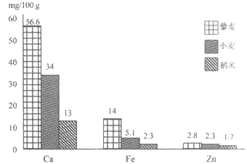
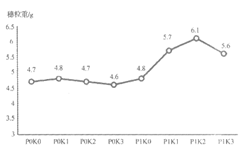
图1 图2
相关实验数据为国内的藜麦种植及推广提供了依据。
请依据文章内容回答下列问题:
(1)藜麦中所含人体必需的营养素有________(任写两种)。
(2)藜麦中的铁元素可以预防________(填”贫血”或”佝偻病”)。
(3)藜麦被列为”全球十大健康营养食品之一”的原因是________。
(4)由图2可知,磷肥、钾肥的最佳施用量为________。
(5)下列说法正确的是_______(填序号)。
A. 藜麦适合减肥人群食用
B. 胆固醇高的人,不适合食用藜麦
C. 藜麦中,钙、铁、锌的含量均高于小麦和稻米
D. 种植藜麦时,施用钾肥的量越大,产量越高
【生产实际分析】
17. (2分)一些光盘的金属层中含有少量银,可通过如下方案回收(其他金属含量过低可忽略)。
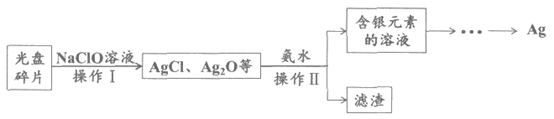
(1)补全化学方程式:4Ag+2NaClO+H2O=2AgCl+Ag2O+□__________。
(2)操作Ⅱ的名称是__________。
18. (3分)硅胶是生活中常用的干燥剂,其生产过程如下图:
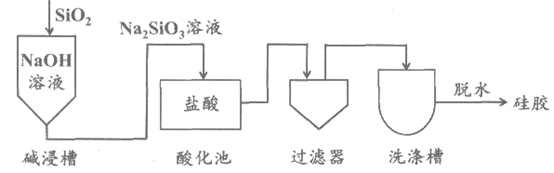
已知:H2SiO3难溶于水。
(1)硅酸钠(Na2SiO3)中硅元素的化合价为__________。
(2)酸化池中发生复分解反应的化学方程式为__________。
(3)上述流程中,洗涤槽的作用是__________。
【基本实验及其原理分析】
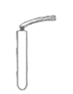
19. (2分)用下图装置进行实验。
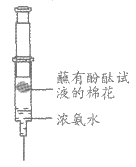
已知:浓氨水显碱性。
(1)实验现象是__________。
(2)该实验说明分子具有的性质是__________。
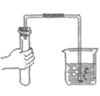
20. (2分)根据下图回答问题。
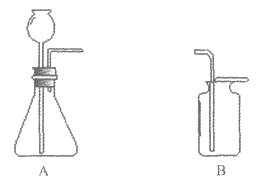
(1)实验室用A装置制备二氧化碳的化学方程式为__________。
(2)用B装置收集二氧化碳,验满的操作是__________。
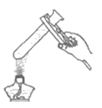
21. (3分)用下图装置验证质量守恒定律。
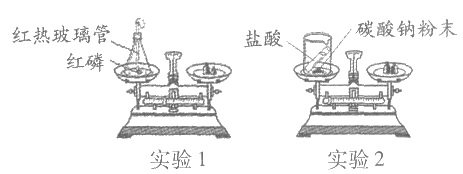
(1)实验1中,发生反应的化学方程式为_________,得出结论所依据的实验现象是_________。
(2)实验2中,天平指针向右偏转,产生此现象的原因是_________。
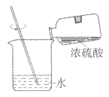
22. (2分)用下图装置验证燃烧的条件。
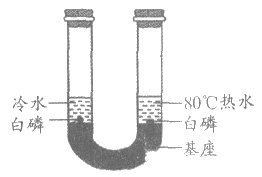
已知:白磷的着火点为40℃。
①将两小块白磷固定在U形管底部基座上,分别加入等体积冷水和热水,白磷均不燃烧。
②一段时间后,将装置倒置。
(1)能证明可燃物燃烧需要温度达到着火点的现象是_________。
(2)该实验_________(填”能”或”不能”)验证与氧气接触是可燃物燃烧的条件之一。
23. (3分)某小组用下图装置探究不同碱溶液吸收二氧化碳的效果。
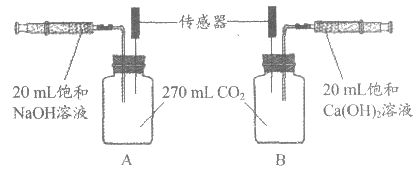
已知:①该实验中,270 mL CO2的质量约为0.5 g;
②20 ℃时,物质的溶解度:NaOH 109 g,Ca(OH)2 0.165 g。
20℃时,分别将注射器中的液体全部快速推入集气瓶。B中集气瓶内溶液先变浑浊后变澄清,压强传感器测定数值如下:
推入液体后压强 | 最终压强 | |
A | 106 KPa | 6.2 KPa |
B | 106 KPa | 103.8 KPa |
(1)A中集气瓶内压强下降的原因是________(用化学方程式表示)。
(2)吸收CO2效果更好的是饱和________溶液(填”NaOH”或”Ca(OH)2“)。
(3)某同学推测,碳酸钙能与水和二氧化碳发生反应生成可溶性物质,依据的现象是________。
【科学探究】
24. (6分)84消毒液(主要成分为次氯酸钠NaClO)可用于物体表面和环境消毒。用钛、石墨等做电极组装简易装置电解食盐水可制备次氯酸钠,能起到一定的应急作用。化学方程式可表示为:NaCl+H2O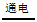 =NaClO+H2↑
=NaClO+H2↑
【提出问题】改变温度、氯化钠溶液浓度、电压和电极间距是否会影响该实验呢?
【查阅资料】有效氯含量可以反映次氯酸钠含量,有效氯含量越高,次氯酸钠含量越高。
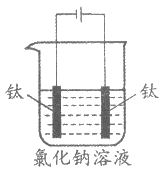
【进行实验】
实验1:20℃,钛电极间距1 cm,电压10 V,1 L氯化钠溶液,通电1小时
实验编号 | 1-1 | 1-2 | 1-3 | 1-4 | 1-5 | 1-6 |
NaCl溶液浓度 | 1% | 2% | 3% | 4% | 5% | 6% |
有效氯含量/(g/L) | 3.5 | 3.8 | 3.9 | 4 | 3.9 | 3.7 |
实验2:1 L 4%氯化钠溶液,通电1小时
实验编号 | 温度/℃ | 电压/V | 钛电极间距/cm | 有效氯含量/(g/L) |
2-1 | 20 | 20 | 1 | 8.4 |
2-2 | 30 | x | 1 | 8.0 |
2-3 | 40 | 20 | 1 | 7.8 |
2-4 | 20 | 20 | 0.5 | 8.2 |
2-5 | 20 | 20 | 1.5 | 8 |
【解释与结论】
(1)由实验1可知,有效氯含量随氯化钠溶液浓度变化的规律是________。
(2)设计实验2-1、2-4、2-5的目的是________。
(3)实验2-2中,x=________。
(4)能证明电压对有效氯含量有影响的实验是________(填实验编号)。
【反思与评价】
(5)实验过程需在通风处进行并严禁烟火,原因是________。
(6)84消毒液对皮肤和口腔黏膜具有腐蚀性和刺激性。一般市售84消毒液有效氯含量为50 g/L,根据使用需要加水稀释成0.2g/L、0.5g/L、1 g/L。结合本实验,下列分析正确的是________(填序号)。
A. 使用84消毒液时建议佩戴防护口罩与手套
B. 本实验中,温度越高,有效氯含量越高
C. 实验2-1中,有效氯含量达到市售84消毒液标准
D. 本实验制备的次氯酸钠溶液需稀释后使用
参考答案
第一部分 选择题
题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
答案 | C | B | C | A | B | A | A | B | D | D | B | C |
第二部分 非选择题
13.
14. (1)BC (2)3CO+Fe2O3
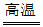 3CO2+2Fe
3CO2+2Fe
15. (1)6:1 (2)B
16. (1)蛋白质、维生素(其他合理答案均可) (2)贫血
(3)藜麦营养成分丰富且比例均衡。
(4)磷肥40千克/公顷,钾肥80千克/公顷。 (5)AC
17. (1)2NaOH (2)过滤
18. (1)+4
(2)Na2SiO3+2HCl=2NaCl+H2SiO3↓
(3)洗去H2SiO3沉淀表面残留滤液
19. (1)棉花变为红色 (2)分子在不断运动
20. (1)CaCO3+2HCl=CaCl2+CO2↑+H2O (2)将燃着木条放于集气瓶口
21. (1)4P+5O2 2P2O5 化学反应前后,天平指针不偏转
2P2O5 化学反应前后,天平指针不偏转
(2)盐酸与碳酸钠反应,生成二氧化碳逸出,烧杯内物质质量减少。
22. (1)装置倒置后,露出冷水的白磷不燃烧,露出热水的白磷燃烧。 (2)能
23. (1)CO2+2NaOH=Na2CO3+H2O (2)NaOH
(3)B中集气瓶内生成的沉淀又消失。
24. (1)其他条件相同时,随着氯化钠溶液浓度从1%到6%,有效氯含量先增大后减小。
(2)探究改变钛电极间距是否影响该实验 (3)20 (4)1-4和2-1
(5)生成可燃性气体氢气,遇明火易爆炸 (6)AD